1. Материалы и методы
БАД Гитагамп-ST – сублингвальные таблетки по 0,1 г.
Состав на 1 таблетку:
Лактоза 94,5 мг
Сорбитол 5,0 мг
Серпуха 1,0 мг
Соли кальция 0,05 мг
(фторид Са, фосфат Са)
Общая масса таблетки 100,05 мг
БАД Гитагамп-ST рекомендована в качестве дополнительного источника фтора и кремния у взрослых. Максимальная суточная доза для взрослых составляет 20 таблеток (2000 мг) или 29 мг/кг.
Экспериментальные исследования проведены на крысятах 3-недельного возраста с первоначальной массой тела 35-40 г при введении в желудок в течение 4 недель.
Лабораторных животных получали и содержали в виварии ВНИИ лекарственных и ароматических растений в соответствии с принятыми санитарными нормами (нормальный световой и температурный режим, свободный доступ к воде, сбалансированный по питательности гранулированный корм и т.д.). Подбор животных в экспериментальные группы осуществляли с учетом родившихся крысят, которых в возрасте 3-недель отсадили от матерей и оставили на самостоятельном вскармливании.
Каждую экспериментальную группу составили 10 крысят: I группа – контроль (интактные), II группа – Гитагамп-ST в дозе 29 мг/кг ( соответственно на крысенка с массой тела 35 г – 1,0 мг), III группа – Гитагамп-ST в дозе 145 мг/кг.
Максимальная испытанная доза являлась 5-кратной рекомендуемой суточной (29 - мг/кг).
Перед введением таблетки растирали в ступке, растворяли в воде и вводили в виде 1-2% растворов в желудок крысятам при помощи зонда в объемах 0,1-0,6 мл на крысенка.
Во время подострого эксперимента у крысят регистрировали выживаемость, прирост массы тела (еженедельно), на 2- и 4- ой неделях регистрировали физическое развитие по общим интегральным показателям и тестам, характеризующим силовую выносливость (время удержания на вертикальном стержне или на краю стола - от начала удержания до момента падения). После 4- недельного введения Гитагампа-ST у крысят из хвостовой вены брали кровь для исследования гематологических показателей периферической крови (общее количество эритроцитов, лейкоцитов, тромбоцитов, содержание гемоглобина, гематокрит, среднее содержание гемоглобина в эритроците, средняя концентрация гемоглобина в эритроците, средний объем эритроцитов, ширина распределения эритроцитов по объему, гемограммы) и биохимических показателей сыворотки крови (общий белок, альбумины, общий холестерин, глюкоза).
Гематологические показатели периферической крови животных определяли на полуавтоматическом гематологическом анализаторе Hema-screen 13 фирмы Hospitex Diagnostics S.A.(Италия). Биохимические показатели сыворотки крови определяли на полуавтоматическом биохимическом анализаторе крови Screen master Tecno фирмы Hospitex Diagnostics S.A.(Италия) при помощи наборов фирмы «Human», Германия.
В конце эксперимента поводили эвтаназию животных в СО2 камере. Взвешивали внутренние органы (сердце, печень, почки, надпочечники, селезенка, семенники), определяли коэффициенты их массы и проводили пагистологические исследования (сердце, семенники, скелетная мышца бедра) общепринятыми методами. Срезы окрашивали гематоксилин-эозином. Исследования проведены в Институте морфологии человека РАН.
Все цифровые данные, полученные в эксперименте, обрабатывали методом вариационной статистики с применением «t» - критерия Стьюдента.
2. Результаты исследования Гитагампа-ST в подостром эксперименте
Как показали результаты исследования, внутрижелудочное введение Гитагампа-ST в течение 4 недель не вызывало изменений общего состояния и поведения крысят. В контрольной и опытной группах крысята нормально развивались, у них сохранялась обычная двигательная активность, опрятный внешний вид, реакция на внешние раздражители. Потребление корма и воды у крысят всех экспериментальных групп не различалось и соответствовало норме. На протяжении всего подострого эксперимента масса тела крысята, получавших Гитагамп-ST в испытанных дозах 29 и 145 мг/кг, была ниже, чем в контроле. На первой неделе эксперимента наблюдали статистически достоверное снижение массы тела крысят в обеих опытных группах по сравнению с контролем. В последующие периоды эксперимента (2 и 3-я недели) отмеченный эффект сохранялся у крысят только III группы, получавших БАД в дозе 145 мг/кг. На 4-ой неделе опыта прирост массы тела крысят, получавших БАД в дозах 29 и 145 мг/кг, был ниже, но не имел статистически значимых различий с контролем (таблица 1).
В течение всего подострого эксперимента в контрольной и опытных группах не отмечено гибели животных.
При изучении влияния БАДа Гитагамп-ST в дозах 29 и 145 мг/кг на силовую выносливость крысят в тесте удержания на вертикальном стержне, показано статистически значимое увеличение исследуемого показателя через 2 и 4 недели эксперимента. В тесте удержания крысят на краю стола выявлены аналогичные результаты, характеризующие увеличение мышечной силы крысят обеих экспериментальных групп, статистически достоверно подтвержденные у животных, получавших максимальную дозу Гитагампа-ST, по сравнению с контролем (таблица 2).
4-недельное внутрижелудочное введение Гитагампа-ST в дозах 29 и 145 мг/кг не изменяло гематологические показатели периферической крови крысят. Количество эритроцитов, тромбоцитов, лейкоцитов, содержание гемоглобина, гематокрит, среднее содержание гемоглобина в эритроците, средняя концентрация гемоглобина в эритроците, средний объем эритроцитов, ширина распределения эритроцитов по объему у животных II и III групп были на уровне показателей в контроле и соответствовали физиологической норме для животных данного вида и возраста (таблица 3).
Исследование биохимических показателей сыворотки крови крысят, получавших Гитагамп-ST в изученных дозах, показало отсутствие статистически значимых изменений в показателях уровня общего белка, альбуминов и глюкозы в сыворотке крови животных II и Ш групп, за исключением статистически достоверного снижения общего холестерина у животных II группы , по сравнению с контролем (таблица 4).
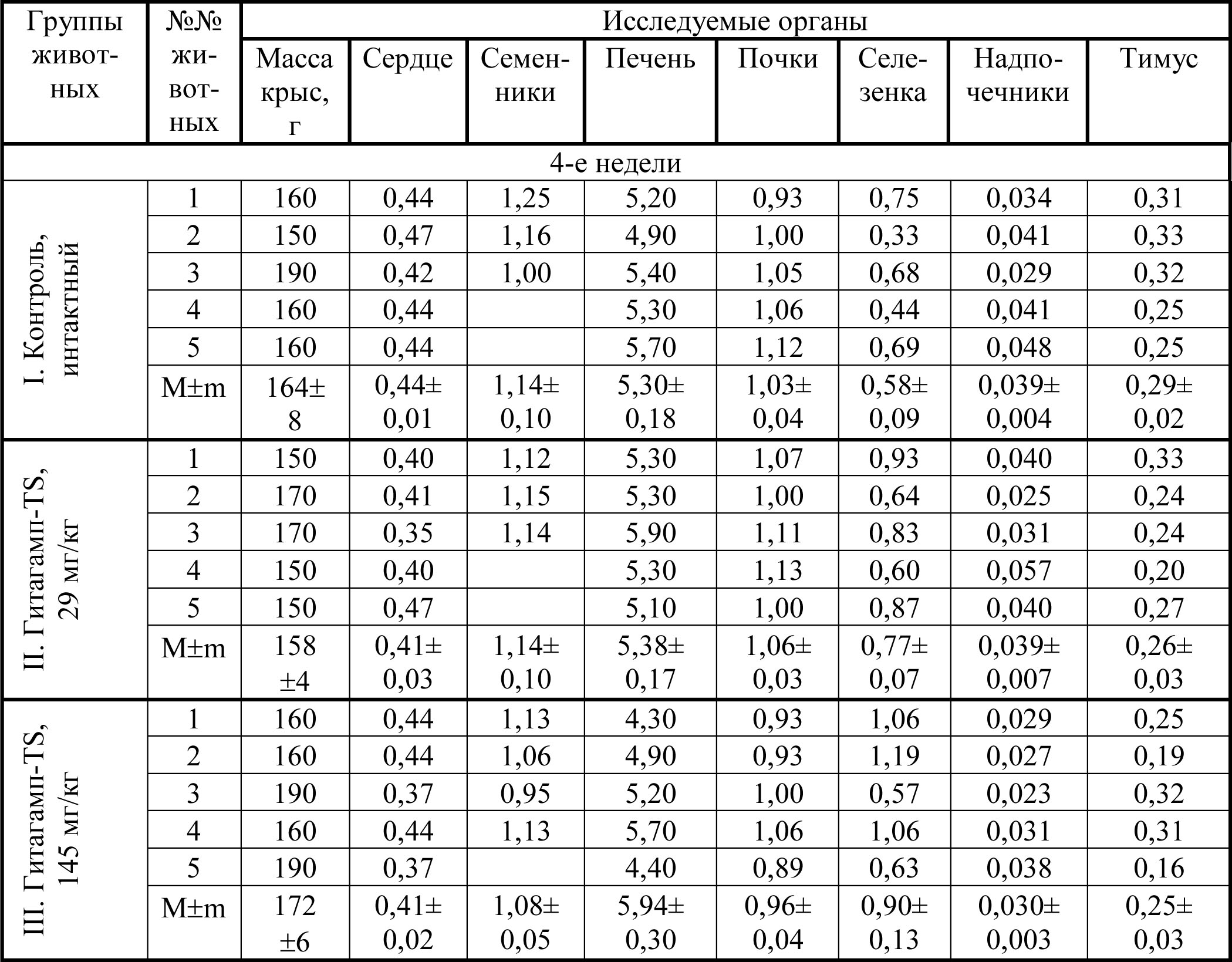
Не отмечено существенного влияния Гитагампа-ST таблеток на
коэффициенты массы внутренних органов (сердце, печень, почки,
надпочечники, семенники тимус) крысят, за исключением дозозависимого
увеличения коэффициента массы селезенки у животных II и III групп по
сравнению с контролем (таблица 5).
Результаты макро- и микроскопического исследования
внутренних органов крысят
Внутренние органы крысят контрольной и опытной групп правильно расположены; полости без выпота и спаек. Серозные оболочки гладкие, блестящие, слизистые - бледно-розовые. Дыхательные пути свободны; легкие эластичны, воздушны, на разрезе обычной окраски. Сердце, печень, почки, селезенка, органы желудочно-кишечного тракта, поджелудочная железа, надпочечники, тимус, семенники, яичники, матка, обычной консистенции, окраски, размеров.
I группа, контроль интактный, №№1-5
Сердце – плотное расположение кардиомиоцитов при адекватной их васкуляризации. На большом увеличении четко видна продольная исчерченность и продолговатые ядра. Среди большинства эозинофильных форм кардиомиоцитов встречаются светлые формы с такой же исчерченностью (№№ 1-5).
Скелетная мышца – на поперечном срезе в мышечных пучках выявляются примерно равные соотношения чередующихся красных и светлых мышц (50:50) (рис. 1) при тесном их расположении и адекватной васкуляризации.
Семенники - на поперечном срезе внутри плотно упакованных канальцев видны сперматогонии типа А, прилегающие к базальной мембране, ближе к просвету – более крупные сперматоциты I порядка и их последующие генерации, встречаются канальцы, содержащие созревающие сперматиды и зрелые сперматозоиды, т.е. эпителиосперматогенный слой соответствует половозрелому возрасту.
II группа, БАД Гитагамп-ST доза 29 мг/кг, №№ 1-5
Сердце – картина миокарда не отличается от интактной группы при таком же количестве светлых кардиомиоцитов (№№ 1-5).
Скелетная мышца – на поперечных и продольных срезах соотношениея красных и светлых мышц 50:50 сохраняется.
Семенники - в отдельных канальцах – разрежение эпителиосперматогенного слоя (№ 2,4,5), у остальных крысят семенники соответствуют норме.
III группа, БАД Гитагамп-ST доза 145 мг/кг, №№ 1-5
Сердце – среди кардиомиоцитов появились разнокалиберные ядра, в наиболее крупных из них – базофилия, особенно в светлых кардиомиоцитах (рис.2) + межуточный отек при адекватной васкуляризации.
Скелетная мышца – соотношения красных и белых мышц разное у животных при общей тенденции увеличения красных гипертрофированных форм (рис.3) + интерстициальный отек.
Патогистологическое заключение
Проведено патоморфологическое исследование внутренних органов крысят контрольной группы (I) и, получавших в течение 4 недель в желудок БАД Гитагамп-ST в дозах 29 и 145 мкг/кг (II и III группы). БАД Гитагамп-ST в дозе 29 мг/кг не вызывает какой-либо перестройки миокардиоцитов и соотношения красных и белых скелетных мышц, кроме начальных изменений в семенных канальцах тестикул. В дозе 145 мг/кг в миокарде отмечается гипертрофия отдельных кардиомиоцитов, а в скелетных мышцах – преобладание красных волокон, с явной гипертрофией отдельных волокон.
ЭКСПЕРИМЕНТАЛЬНОЕ ИЗУЧЕНИЕ СПЕЦИФИЧЕСКОЙ ФАРМАКОЛОГИЧЕСКОЙ АКТИВНОСТИ БАДа ГИТАГАМП-ST
таблетки по 0,1 г
в виде таблиц №№ 1-5
Таблица 1
Динамика массы тела крысят (в % к исходной), получавших внутрижелудочно Гитагамп-ST в подостром эксперименте
Исходная масса тела крысят в г
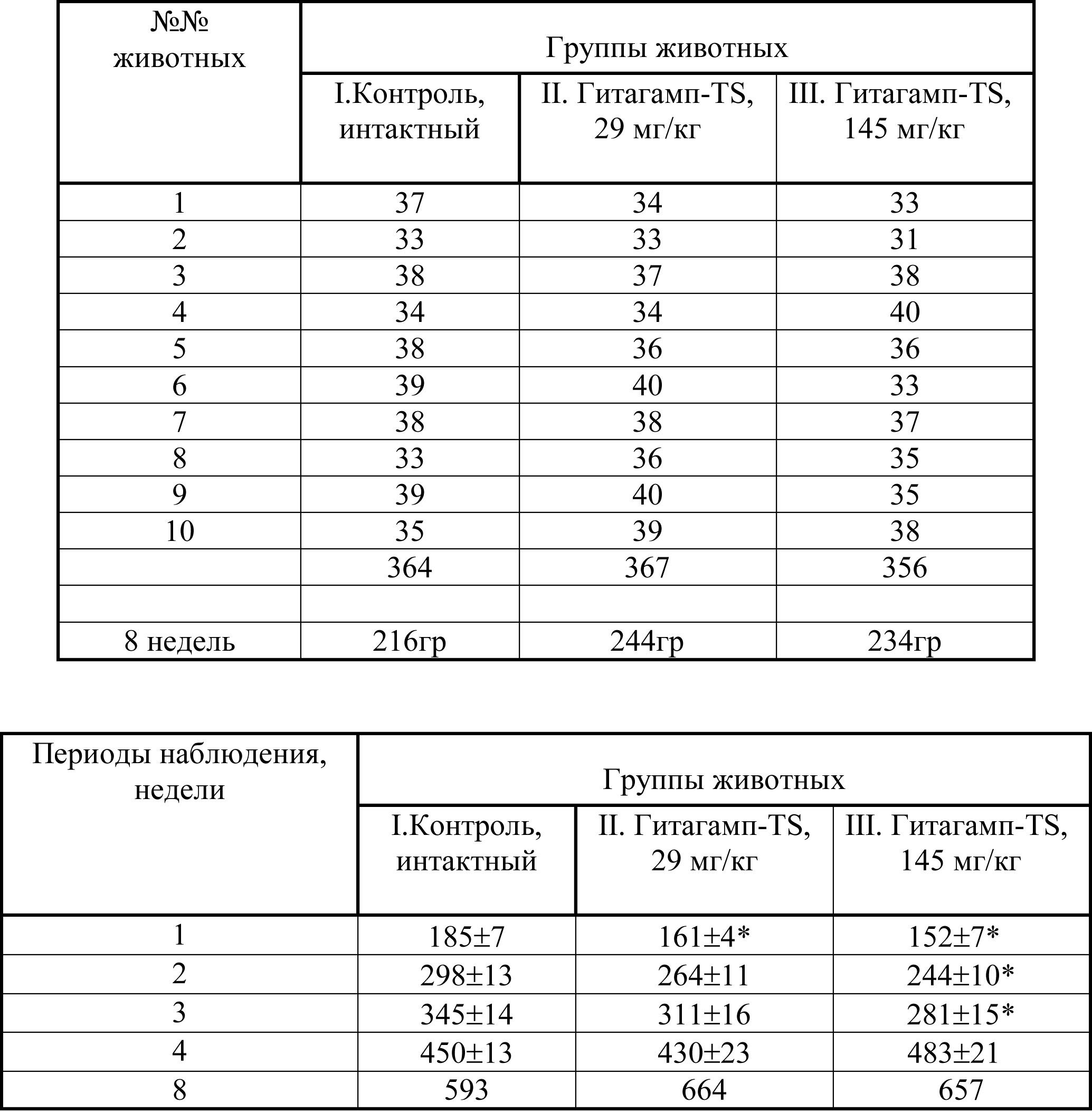
* здесь и в последующих таблицах – достоверность различий с контролем (Р<0,05)
Таблица 2
Показатели периферической крови крысят, получавших внутрижелудочно Гитагамп-ST в подостром эксперименте
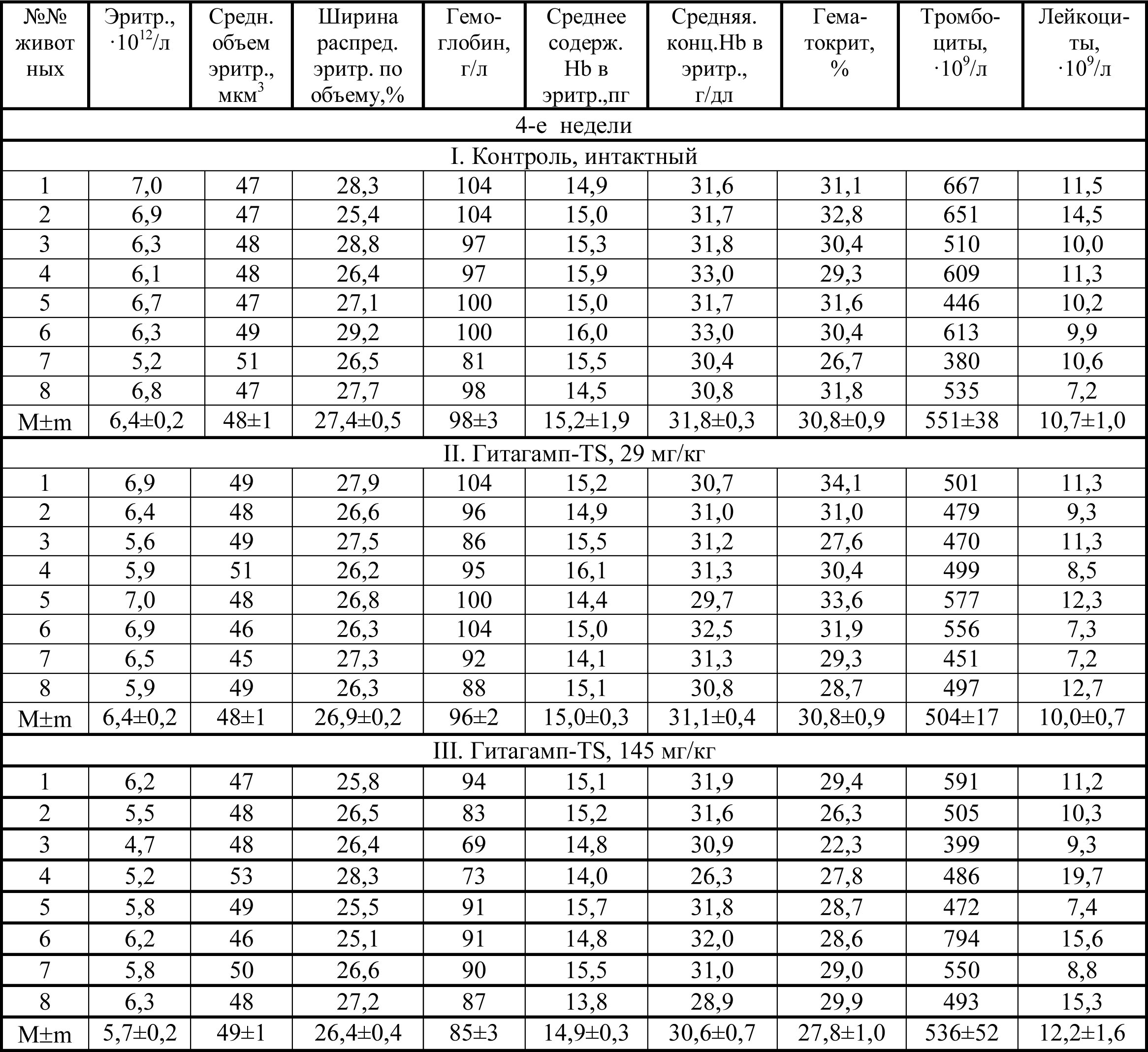
Таблица 3
Биохимические показатели крови крысят, получавших внутрижелудочно Гитагамп-ST в подостром эксперименте
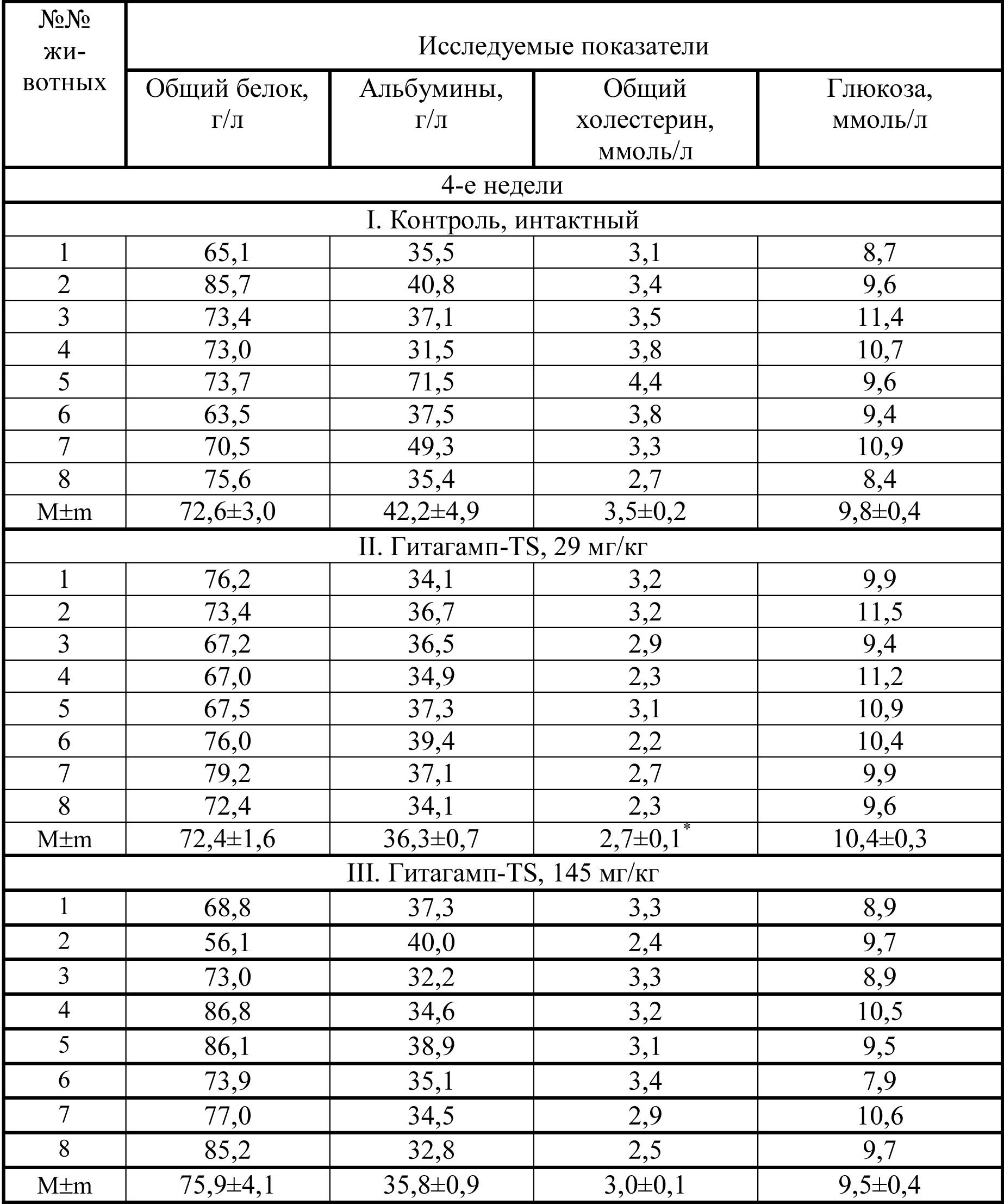
Таблица 4
Показатели мышечной силы крыс, получавших внутрижелудочно
Гитагамп-ST в подостром эксперименте
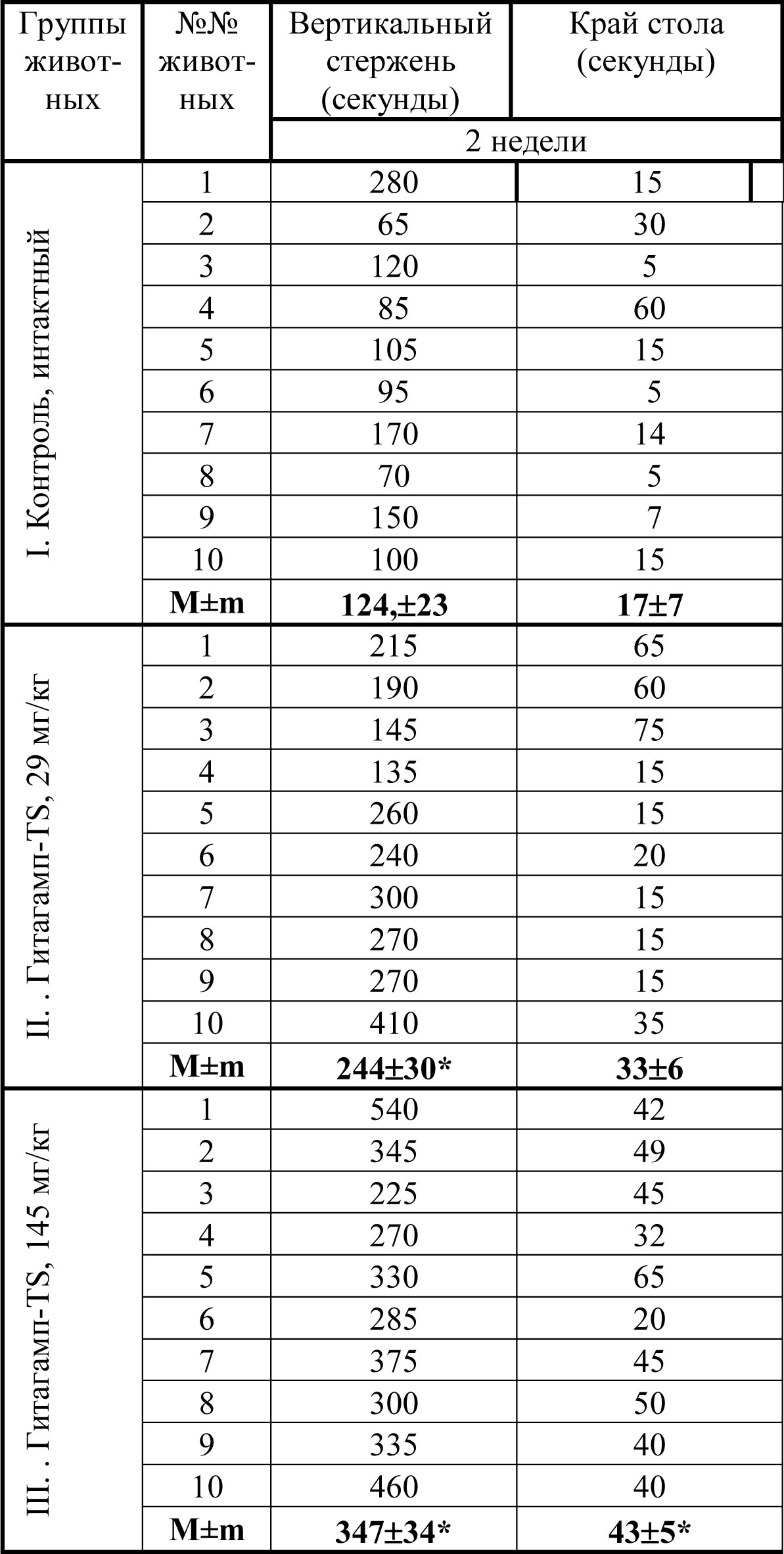
Таблица 4 (продолжение)
Показатели мышечной силы крыс, получавших внутрижелудочно
Гитагамп-ST в подостром эксперименте
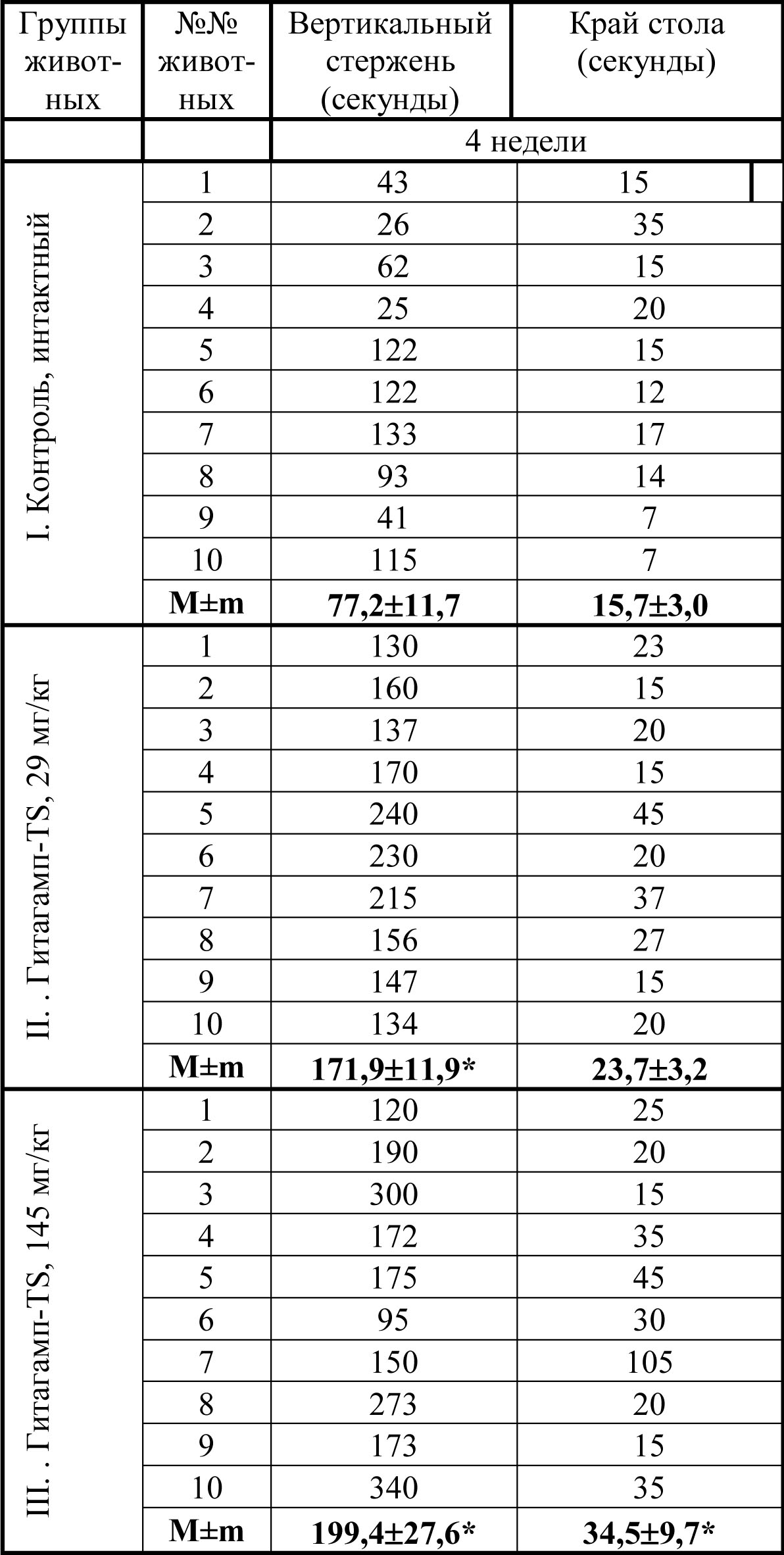
Таблица 5
Коэффициенты массы внутренних органов крыс
(масса органа в г на 100 г массы тела), получавших внутрижелудочно Гитагамп-ST в подостром эксперименте